Prof. Dr. Ayhan DİNÇKAN
Karaciğer
Naklinin
Komplikasyonları
Enfeksiyon karaciğer nakli hastalarının %60-80’ini etkiler!
Karaciğer Naklinin Komplikasyonları
Karaciğer nakli son dönem karaciğer hastalığı, akut irreversibl karaciğer yetmezliği ve seçilmiş vakalardaki hepatik malignitelerde tercih edilen seçkin bir tedavi yöntemidir. Ancak bu yaklaşımın kabul edilebilir komplikasyonları vardır. Karaciğer naklinden önce son dönem karaciğer hastalarının sağkalım süresi aylarla ifade edilirken, nakil sonrasında bu süre çok uzatılmıştır. Son yıllarda cerrahi teknikteki ve anestezi protokollerindeki gelişmeler ile yeni immunsupresif rejimlerdeki ilerlemelere bağlı olarak 1 yıllık hasta sağkalım oranları deneyimli merkezlerde % 90’ların üzerine çıkmıştır. Ameliyat sonrası yinede yüksek mortalite oranına sahip 1 yıldan sonra, hasta sağkalımı daha da artmakta ve yaşam kalitesi düzelmektedir.

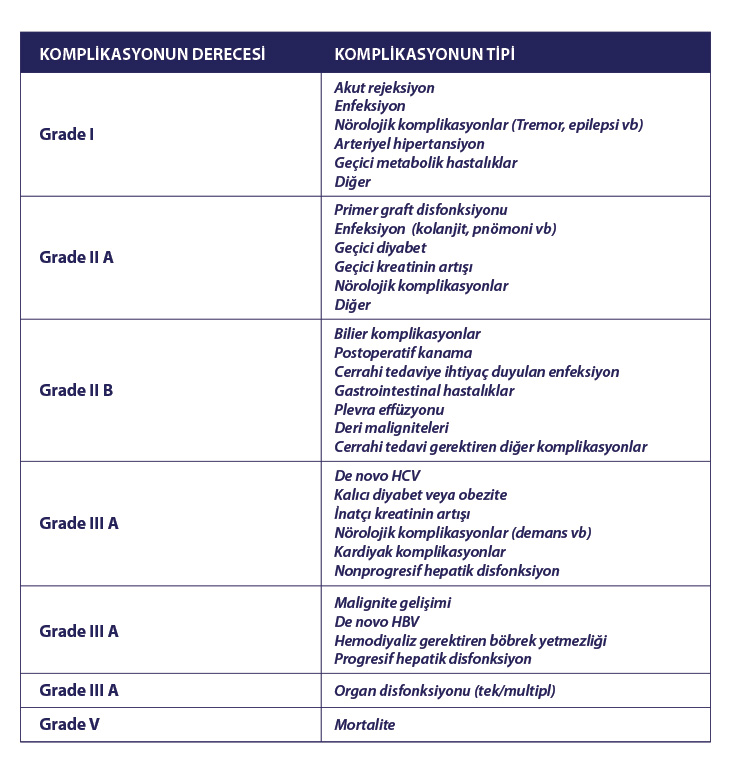
Bu komplike cerrahinin greft ve hasta kaybına neden olan erken ve geç dönem komplikasyonları mevcuttur. Erken postoperatif dönemin gidişini etkileyen en önemli faktör, gelişen komplikasyonların sayısıdır. Bunlar arasında inferior vena kavadan (VCİ) daha ziyade hepatik arter veya portal veni içeren vasküler komplikasyonlar yüksek mortalite ve morbiditeye neden olmaktadır. Geç dönem hasta kayıplarının en önemli sebepleri ise kardiyovasküler hastalıklar veya immunsüpresyona bağlı gelişen enfeksiyon ve maligniteler olarak gösterilmektedir. Dolayısı ile karaciğer nakli sonrası hasta sağkalımını arttırmanın en önemli yolu medikal ve cerrahi komplikasyonların erken tanı ve tedavisini sağlamak ile immunsupresyondaki gelişmelere bağlıdır. Karaciğer nakli sonrasında ortaya çıkan istenmeyen komplikasyonlar Clavien Sınıflandırma Sistemi kullanılarak derecelendirilebilir.
Bu sistemde, grade 1 istenmeyen yan etkiler, farmakolojik veya cerrahi tedavi ya da endoskopik veya radyolojik girişim gerektirmeyen, ameliyat sonrası olağan süreçte sapmaya neden olan komplikasyonları içermektedir. Grade 2 komplikasyonlar, farmakolojik tedavi gerektiren grade 1 koplikasyonlardır. Grade 3 olanlar, genel anestezi gerektirmeyen (3a) veya gerektiren (3b) cerrahi tedaviye ihtiyaç doğuran durumları içermektedir. Grade 4, tek organ disfonksiyonu (4a) veya çoklu organ disfonksiyonu (4b) nedeniyle yoğun bakım ünitesine ihtiyaç duyulan durumlar, beşinci derece ise ölüme neden olan durumlardır. Bu sınıflamanın avantajı hafif, şiddetli ve hayatı tehdit eden komplikasyonlar arasındaki farkı standardize etmektir. Dolayısı ile bu standardizasyon çeşitli merkezler arasındaki verilerin karşılaştırılmasına olanak tanır.
Karaciğer Nakli Sonrası Komplikasyonların Sınıflaması
Vasküler Komplikasyonlar:
Ortotopik karaciğer transplantasyonunun (OLT) vasküler trombozları morbidite ile hasta ve allograft sağkalımını etkileyen en önemli komplikasyonlardır. Bunlar vasküler anastamozların (infrahepatik ve suprahepatik vena kava, hepatik arter ve portal ven) birinde ortaya çıkabilen kanama, stenoz ve tromboz olmakla birlikte en çok görülen komplikasyon hepatik arter ve portal vende görülen trombozdur.
Hepatik Arter Trombozu:
Hepatik arter trombozu (HAT) OLT sonra erken dönem graft kaybının en sık sebebi olup, değişik erişkin serilerinde %2- %20 arasında görülmektedir. Pediatrik karaciğer naklinden sonra özelliklede canlı donör nakillerde damarların küçük çapta olması ve düşük alıcı ağırlığı nedeni ile yetişkinlere oranla daha fazla (%25- 40) rapor edilmektedir. HAT ile ilişkili genel faktörler hepatik arter duvarının diseksiyonu, anastomozun teknik yetersizliği, hepatik arter çapının 3 mmden daha küçük olması, median arkuat ligamana bağlı çeliak stenoz veya kompresyon, aksesuar alıcı veya donör arter anatomisi, allograftın karmaşık backtable rekonstrüksiyonu ile arterioplasti (mikrovasküler rekonstrüksiyon) ve rejeksiyon veya ciddi iskemi-reperfüzyon hasarına bağlı ortaya çıkan yüksek dirençli mikrovasküler arterial akım olabilmektedir. Alıcı-verici ağırlık oranının 1.25’ten küçük olması, uzamış soğuk iskemi zamanı, ABO uyumsuzluğu, verici pozitif – alıcı negatif CMV durumu, kuagülasyon anomalileri (protein C ve S eksikliği, antitrombin III ve antifosfolipid sendromları) ve sigara içimide HAT riskini arttırabilmektedir. Diğer nadir sebepler arasında; hepatocellüler karsinoma (HCC) tedavisinde kullanılan transarteriyel kemoembolizasyonun yarattığı periarteriyel inflamasyon ve fragilite, malignite ile ilişkili hiperkuagulobilite durumu sayılmaktadır. Cerrahi teknikteki ilerlemelerin HAT insidansını azaltmasına rağmen, hala hasta ve graft sağkalımını ciddi anlamda tehdit etmekte olup, HAT’ın mortalitesi %50- 60 arasındadır, re-transplantasyon yapılmadığı zaman mortalite % 73’e yükselmektedir.
HAT çok değişik klinik ve laboratuar sonuçları ile karşımıza çıkabilmekte ve hastaların çoğunda nonspesifik olabilmektedir. 4 değişik klinik formda karşımıza çıkar; 1- Nekroz varlığı, 2- Enfeksiyon formu, 3- Bilier komplikasyonların ön planda olduğu form ve 4- Asemptomatik formdur. Erken dönemde olan akut trombozlarda ateş, lökositoz, graft yetmezliği, bilier nekroz ve kaçakları gelişmekte ve rekonstrüksiyon yapılmazsa retransplantasyon gerektiren ciddi klinik tablo yanında, daha nadiren parankimde gelişen iskemiye bağlı transaminaz yüksekliğide görülebilmektedir. Geç dönem trombozlarda cerrahiden aylar yada yıllar sonra safra kaçağı, safra yolu striktürleri ve tekrarlayan bakteriyemi ve sepsis arası değişen klinik durumlar görülmekle birlikte, geç dönem HAT’ nın 1/3’ünde cerrahi girişim gerekmemektedir. Erken ve geç dönemin zamanı konusunda fikir birliği olmamakla birlikte, OLT sonrası ilk 30 gün içinde gelişen HAT erken dönem komplikasyon olarak kabul edilmektedir. HAT tedavisi genellikle reeksplorasyon, cerrahi trombektomi ve anastamoz revizyonunu içermektedir. Revizyonların başarısız olduğu durumlarda da hayat kurtarıcı prosedür retransplantasyon olmaktadır. Risk belirlemek için bazı otörler intraoperatif hepatik arter kan akımı ölçümünü kullanmışlar ve akım 400 mL/dk altında olanlarda HAT riskinin arttığını ifade etmişlerdir. HAT erken teşhisi hayat kurtarıcı olup, bunun için en az günde 2 kez postoperatif 7- 14 gün arasında rutin doppler incelemesi önerilebilir. Dolayısı ile erken trombektomi ile erken ve geç dönem komplikasyonlar ile hatta mortaliteden kaçınılmış olur.
Hepatik Arter Stenozu:
Hepatik arter stenozu (HAS) genellikle anastamoz hattında veya nativ arterdeki klemp hasarına bağlı olarak gelişmektedir. Karaciğer enzimlerinde yükselme, bilier komplikasyon gelişmesi veya başka sebeplerle yapılan doppler incelemede insidental olarak saptanabilir. HAS şüphesi devam ederse selektif hepatik anjiografi ile doğrulamak gerekir. Erken postoperatif dönemde saptanırsa cerrahi trombektomi yapılmalıdır. Alıcı damar sisteminde sorun varsa donör arter konduitleri ile vasküler greft konulması gerekebilir. Trombektomi ve rekonstrüksiyonlar ile akım sağlanamaz ise retransplantasyon gerekir. Geç dönem HAS da selektif anjiografi ve balon anjioplasti ile tedavi edilebilmektedir.
Hepatik Arter Psödoanevrizması:
Seyrek ancak hayatı tehtid eden bir komplikasyondur. İnfekte bilioma veya arteriyel greft ile rekonstrüksiyon en önemli etyolojik sebeplerdir. İntraperitoneal rüptür ile masif kanamaya yol açabilir. Tedavide ise homogreft kullanılarak yapılan cerrahi rezeksiyon-rekonstrüksiyon veya stent yerleştirilmesi yapılabilmektedir.
Portal Ven Trombozu:
Portal ven trombozu (PVT) erişkin OLT’dan sonra %1- 7 arasında görülürken, pediatrik nakillerden sonra %11 oranında rapor edilmektedir. HAT da olduğu gibi hasta ve graft içinde fatal olabilmektedir. Posttransplant PVT ile ilişkili faktörler portal venin bol tutulması, nakil esnasında trombovenektomi ihtiyacı (nakil öncesi PVT olması), portal ven çapının küçüklüğü (<5 mm), çap uygunsuzluğu, yanlış açılanma, türbulan akıma neden olabilecek burs dikiş atılması, erken yapılan splenektomi, portal ven rekonstrüksiyonu için venöz conduit kullanılması ve pediatrik alıcılardaki portal ven hipoplazisi olarak sayılabilir.
PVT klinik olarak karşımıza gastrointestinal kanama, asit, transaminaz yüksekliği ve akut graft yetmezliği gibi portal hipertansiyon bulguları ile çıkabilir. Bazı çalışmalarda ise hastaların yarıya yakınında (%43) portal ven trombozunun asemptomatik olduğu, dolayısı ile karaciğer fonksiyonlarında değeşiklik olmadığı saptanmıştır. Doppler ultrasonografi tanıda kullanılan ilk seçenek olup, anjiografi ile tanı doğrulanabilir.
PVT ilk seçenek stentli veya stentsiz perkütan transluminal anjioplasti denenebilir. Ancak bu komplikasyonun klasik tedavisi HAT’da olduğu gibi eksplorasyon, cerrahi trombektomi veya anastomoz revizyonudur. Revizyonun başarısız olduğu durumlarda retransplantasyon kaçınılmazdır. Güncel tedavi olarak kateter konularak veya medikal antikuagulan veya trombolitik uygulamalar denenmekte fakat gerek HAT, gereksede PVT da hasta ve graft sağkalımına etkisi gösterilememiştir. PVT için retransplant yapılan hastalarda hepatotrofik faktörleri sağlayan potent bir mezenterik graft ihtiyacı vardır. Ekstensive PVT olan olgularda venöz konduit kullanılsa bile retransplant her zaman mümkün olmayabilir. PVT önleyebilmek için önerilen cerrahi teknikler küçük venler için aralıklı sutur ile yapılan venoplasti, anastamozda gerginlik veya bolluktan kaçınılması, yeterli portal akımın sağlanması ve portal venin nazik manuplasyonu olarak gösterilebilir. PVT için en önemli risk faktörlerinden biri recipient portal venin çap küçüklüğü olduğu için tüm pediatrik alıcılarda post-OLT sonrası antikuagülasyon önerilmektedir. Karaciğer naklinden sonra vasküler tromboz için kontrol edilebilir risk faktörleri olan hiperkuagülasyon, hipovolemi ve graft kompresyonundan kaçınılması gerekir.
Vena Cava Anastamozu Komplikasyonları
Vena kava anastomozuna bağlı stenoz veya oklüzyon gibi hepatik outflow komplikasyonları nadir olmakla birlikte görüldüğü zaman ciddi sonuçları olabilmektedir. Karaciğer naklinden sonra kaval anastomoz komplikasyonu görülme insidansı cerrahi tekniğe bağlıdır. Bikaval anastomozun kullanıldığı konvansiyonel teknikte kaval obstrüksiyon görülme insidansı %1- 2 arasındadır. Yakın geçmişte tarif edilen ve tek kaval anastomozun kullanıldığı Piggy-back tekniğinde bu oran %4 oranında olup, daha yüksektir. Canlı donör split karaciğer nakillerinde de hepatik outflow riski % 2-4 oranında bildirilmekte olup bu kadavra vericili tam karaciğer nakillerine göre daha fazladır. Etyolojide alıcı verici uygunsuzluğuna bağlı greft rotasyonu, hiperkuagulopatiye bağlı alt kava trombozu, anastomoz hattı sütürlerinin sıkı olması, redundan hepatik venin katlantı yapması, anastomoz esnasında arka duvardan dikiş geçilmesi, büyük greftin kaval kompresyona neden olması ve alıcı tarafında üç yerine iki hepatik ven orifisinin kullanılmasıerken dönemde, anastomoz hattında fibrozis veya intimal hiperplazi ise geç dönem komplikasyonlardan sorumludur. Klinikte hepatik outflow sorunu karşımıza yeni başlayan masif asit, alt ekstremite ödemi, varis kanaması, splenomegali, renal yetmezlik, greft disfonksiyonu ve hatta greft kaybı ile karşımıza çıkabilir. Radyolojik olarak CT, MR anjiografi ve doppler ultrasonografiden yararlanılır. Ancak venografi hala altın standart yöntemdir. Genellikle hepatik ven veya vena kava darlıklarında noninvaziv balon anjioplasti veya metal genişleyebilen stentler ile tedavide kullanılmaktadır.
Bilier Komplikasyonlar:
Bilier sistem komplikasyonları gerek erken dönem gerek geç dönemde karaciğer naklinden sonra sık görülen mortalite ve morbiditeye neden olan komplikasyonlardan biridir. Bu nedenle safra yolları rekonstrüksiyonunun karaciğer naklinin ‘’Achille tendonu’’ olduğu ifade edilmiştir. Nakillerin ilk vakalarında baş belası olup, karaciğer nakli hastalarının yaklaşık üçte birinde meydana gelmiştir. Safra ağacı kanlanmasının daha iyi anlaşılması, cerrahi teknikteki gelişmeler ve absorbabl sütür materyallerinin kullanılması ile bu komplikasyon oranları %9- 15 arası bildirilmektedir. Bu oranlar canlı donör karaciğer alıcılarında daha yüksek gösterilmekle birlikte çoğu yazara göre bu oranlar %22- 64 arasında değişmektedir. Çoğu bilier komplikasyon ameliyattan sonraki ilk 2-3 ay içinde görülmektedir. Transplant alıcılarında yaklaşık %1- 3 oranında greft kaybına neden olarak graft ve hasta için risk oluşturmaktadır. Safra yolu komplikasyonlarının etyolojisi multifaktöriyeldir. Safra yolu darlıkları ve kaçaklarının sebebi genel olarak hatalı rekonstrüksiyon metoduna, teknik olarak yetersiz anastamoza ve kötü organ prezervasyonu esnasındaki safra yolu yaralanmasına bağlıdır. En önemlisi safra yolları kan akımının azlığı veya olmamasıdır. Çünkü transekte edilen donör safra yolunun tek kan akımı kaynağı karaciğerden gelen akımdır. Dolayısı ile koledok anastamozunun mümkün olduğunca sistik kanal güdüğünün proksimaline yapılması önerilebilir. Bunun dışında diğer etyolojik faktörler olarak; uzamış soğuk ve sıcak iskemi süreleri, oddi sfinkter disfonksiyonu, CMV enfeksiyonu, vasküler rejeksiyon ve ABO uyumsuzluğu sayılabilmektedir. Primer sklerozan kolanjit tanısı olan hastalarda safra yolu komplikasyon oranı daha fazladır. Bunların dışında değişik serilerde %1- 9 oranında görülen ve hepatik arter trombozu ve diğer sebepler olmaksızın ortaya çıkabilen nonanastomotik bilier striktürler görülebilir. Bu tür komplikasyonlar çok yıpratıcı olabilir çünkü sebebi bilinmemekte, safra ağacının pek çok yerinde görülebilmekte ve tedavisi de zor olabilmektedir. Genellikle intrahepatik striktür ve dilatasyon şeklinde bilier lezyonlar olarak görülmektedir.
Erken dönem komplikasyonlar safra kaçakları ve anastomoz darlıklarından meydana gelir. Kaçaklar genellikle anastomozdan kaynaklanmakla birlikte donör ve alıcı sistik kanal stump undan, reduced size graftların kesi yüzeyinden ve T-tüp kullanılmış ise bunun safra yolu çıkış yerinden de olabilmektedir. Hemen hemen bütün kaçaklar teknik sebeplerden olmakla birlikte anastomoz kaçakları esas olarak safra yolu ucunun (en fazla donör tarafında) iskemik nekrozundan veya teknik olarak yetersiz anastomoza bağlıdır. Geç dönem bilier komplikasyonlar transplanttan sonra aylar veya yıllar içerisinde gelişir. Bunlar genellikle erken dönem komplikasyonların tekrarlaması veya tam olarak tedavi edilmemesinden meydana gelir. Bu anlamda kaçaklar, intrahepatik biliomalar ve safra yolu darlıkları genel olarak görülebilenlerdir. Kronik bilier problemleri hepatik arter trombozu zemininde gelişirse tedavisi zor olabilmektedir.
Klinik olarak karın ağrısı, bulantı-kusma, ateş ve sarılık bulguları bilier sistem komplikasyonlarında karşımıza çıkar. Laboratuarda bilurubin, alkalen fosfataz ve gama glutaril transferaz yüksekliği saptanabilir. Tanıda doppler ultrasonografi, HİDA-sintigrafisi, tomografi gibi abdominal görüntüleme yöntemleri veya ERCP, perkütan transhepatik kolanjiografi veya varsa T-tüp kolanjiografi gibi kolanjiografik çalışmalar kullanılmaktadır. ERCP’nin sfinkterotomi ve internal stent yerleştirilmesi gibi tedavi edici avantajlarıda vardır. Donör safra ağacına bağlı meydana gelen komplikasyonlarda hepatik arterin açıklığı (doppler ultrasonografi veya CT-anjiografi) mutlaka gösterilmelidir.
Erken ve geç dönem komplikasyonların tedavisinde ilk tercih perkütan veya endoskopik olarak yapılan internal veya eksternal drenaj girişimleridir. Deneyimli ellerde bu girişimlerin başarısı artmaktadır. Geç dönem komplikasyonların doğası ve uzamış darlığı nedeni ile, tanı çalışmalarında gösterilen büyük defektlerde ve başarısız perkütan girişimlerden sonra cerrahi tedaviler kaçınılmaz olur. Kompleks hiler ve intrahepatik darlıkların cerrahi dışı yöntemlerle tedavisi zordur. Bu durumda cerrahi revizyon veya retransplantasyon gibi definitiv cerrahi yöntemlere ihtiyaç duyulabilir.
Primer Nonfonksiyon:
Karaciğer nakli sonrası primer nonfonksiyon yeni takılan graftın fonksiyon görmediği zaman hayatı tehtid eden en enemli komplikasyonudur. Karaciğerin revaskülarizasyonu ile başlar, retransplantasyon veya hasta kaybı ile sonlanır. İnsidansı bütün karaciğer nakillerinde % 1.8- 14 (% 2-20) arasında değişmektedir. Tanısında graft karaciğerin vasküler yapılarının normal olduğu bertaraf edildikten sonra klinik ve laboratuar değerlendirmesi ile konur. Primer nonfonksiyonda hafif bir fonksiyon bozukluğundan, transaminazlarda ani artış (3000> U/mL), safra yapımının olmaması, ciddi karaciğer ilişkili kuagulopati, laktat seviyesinde artış, metabolik asidoz, hipoglisemi ve hemodinamik instabilite gibi ağır tablo ile karşımıza çıkabilir. Hastalar hızla ağır ve ilerleyici böbrek, akciğer, nörolojik ve kalp yetmezliğine gider. Patolojik olarak karaciğer allograft biyopsisinde hepatik sitolizis, kuagülasyon nekrozu vardır. Primer nonfonksiyonun kesin etyolojisi tam olarak bilinmemekle birlikte, uzamış soğuk iskemi zamanı, kadın donör cinsiyeti, donör yaşının ileri olması, donörün yoğun bakımda kalması, kardiyak ölümlü donörden alınan karaciğerin kullanımı, transplantasyon prosedürünün uzaması, karaciğer grefttinde yağlı değişiklikler, greft boyutunun küçüklüğü ve alıcıdaki böbrek yetmezliği risk faktörleridir. Primer nonfonksiyon geliştiğinde acil retransplantasyon yapılmadığı zaman mortalite ile sonuçlanır. Bunun yanında prostoglandin E1, immunoferezis, moleküler adsorbent recirculating sistem (MARS) ve total allograft hepatektomi ve geçici portakaval şant gibi ek destekleyici tedaviler bazı gruplarca önerilmektedir. Ancak günümüzde primer nonfonksiyon gelişeceğini belirleyecek kesin bir faktör veya gelişimini engelleyecek herhangi bir farmakolojik ve cerrahi yöntem bildirilmemiştir. Dolayısı ile bu mortal komplikasyondan korunmanın tek yolu gelişimini engellemek, geliştiğinde de erken tanıyıp, acil retransplantasyon yapmaktır.
Greft Rejeksiyonu:
Karaciğer nakillerinde de rejeksiyon klasik olarak hiperakut veya antikor ilişkili rejeksiyon, akut veya hücresel rejeksiyon ve kronik veya duktopenik rejeksiyon şeklinde üç kategoride incelenir. Hiperakut rejeksiyon hepatik allograft rejeksiyonunun çok nadir bir formudur ve transplante karaciğer ile alıcı antikorlarının karşılaşması ile hızla başlar ve ilk 3 hafta içinde de görülebilir. Akut rejeksiyon ilk olarak nakli takiben 5-7 gün içinde oluşur ve ilk 90 gün içinde en sık görülür. Yıllar sonrada görülebilir. Burada normal giden bir karaciğeri kontrol dışı kalan T hücrelerinin başlattığı olaylar sonucunda graft hasarı olmaktadır. Kronik rejeksiyon ise ilk olarak nakli takiben haftalar içinde görülmekle birlikte, yıllar sonrada ortaya çıkabilmektedir. Safra yollarına immun saldırı sonucu iskemik hasarı ile karakterize olduğu için duktopenik veya ‘’yokolan safra yolu sendromu= vanishing bile duct’’ olarak isimlendirilir. Kliniğinde kolestaz ön planda olup, histolojik olarak safra kanalı azlığı veya kaybı sözkonusudur. Rejeksiyon gelişimi açısından karaciğer diğer solid organlardan daha şanslıdır. Bunun nedeni diğer organlara göre daha az antijenik yapıya sahip olmasıdır. Böbrek gibi damar endotelinden zengin bir yapıdan ziyade venöz yapının daha hakim olduğu sinuzoidal boşluklardan oluşmaktadır. Bu nedenle antikor bağımlı rejeksiyon ihtimali daha azdır. Klinik karaciğer nakillerinde kalsinörin inhibitörlerinin (1980’lerde siklosporin, 1990’larda tacrolimus) kullanılmasından beri graft ve hasta sağkalımlarında dramatik bir iyileşme sağlanmıştır. Ancak kalsinörin inhibitörlerinin yan etkileri uzun dönem sonuçları olumsuz etkilemektedir. Kalsinörin inhibitörleri ve steroidler ciddi anlamda metabolik, renal ve kardiyovasküler komplikasyonlar ile ilişkilidir. Bu nedenle günümüzde uzun dönem sağkalımı arttırmak için yapılan major değişiklik uzun dönem toksisiteyi azaltmak ve graft uyumu ile hasta yaşam kalitesini arttırmak amacı ile değişik immunsupresif ajanların (mikofenolate mofetil ve sirolimus) kullanımı denenmektedir. Tüm bu gelişmelere rağmen karaciğer nakli sonrası akut rejeksiyon oranı %20-60 oranında görülmektedir. Tanı klinik, laboratuar ve histopatolojik inceleme yani biyopsi ile konur. Hiperakut rejeksiyonun tedavisi retransplantasyondur. Akut rejeksiyon ise ilaçlarla (yüksek doz steroid, monoklonal-OKT 3 veya poliklonal antikorlar-ATG) tedavi edilmekte, nadiren greft kaybına neden olmaktadır. Günümüzde yokolan safra yolu sendromu yani kronik rejeksiyon geliştiğinde immunsupresyon değişikliğine cevap vermediği için tek tedavi şekli retransplantasyondur.
Böbrek yetmezliği:
Karaciğer nakli sonrası böbrek yetmezliği ameliyattan sonra akut ortaya çıkan ve geç dönemde ortaya çıkan kronik yetmezlik şeklinde görülmektedir. Ameliyat sonrası ortaya çıkan akut böbrek yetmezliği karaciğer nakillerinden sonra pek çok merkezde değişik oranlarda (%12- 61) görülebilmektedir. Akut böbrek yetmezliğinin nedeni genellikle akut tubüler nekrozdur. İnsidans ile ilişkili faktörler olarak; diyabet varlığı, asit, hepatik ensefalopati, renal fonksiyonları bozacak olan kan transfüzyonu sayısı, kan kaybı, operasyon esnasında uzamış iskemi, reoperasyon gerekliliği, nakil sonrası kalsinörin kullanılması ve ciddi enfeksiyonlar sayılabilir. Akut böbrek yetmezliği gelişen hastalarda postoperatif mortalite oranı (ilk 30 gün içinde) böbrek yetmezliği gelişmeyenlerden daha fazladır.Bu komplikasyonun gelişiminin önlenmesi için intraoperatif ve postoperatif kan ve sıvı kayıplarının yeterli düzeyde replase edilerek renal perfüzyonun korunması sağlanmalıdır. Erken postoperatif dönemde görülen akut böbrek yetmezliği vakalarının çoğu uygun tedavilerle iyileşirken bazı vakalarda böbrek yetmezliği kalıcı ve terminal dönem böbrek yetmezliği ile sonuçlanabilmektedir.
Renal disfonksiyon veya son dönme böbrek yetmezliği karaciğer naklinin en sık geç dönem komplikasyonlarındandır ve hasta ve greft sağkalımını etkileyen en önemlili faktörlerden biridir. Nakil sonrası 5 yıllık takipte renal disfonksiyon yani GFR hızının 40 ml/dk altında saptanma oranı % 27 iken, 10 yıllık takipte son dönem böbrek yetmezliği saptanma oranı %10 olarak saptanmıştır. Pretransplant renal disfonksiyon nakil sonrası kronik böbrek yetmezliğinin en önemli nedeni olup diğer faktörler ise önceden varolan diyabet/hipertansiyon varlığı, transplant esnasında akut böbrek hasarı ve diğer en önemli nedeni kalsinörin inhibitörlerinin kullanımına bağlı nefrotoksisite sayılabilir. Bu durumda kalsinörin inhibitörlerinin dozunun azaltılması yanında, tamamen kesilerek diğer immunsüpresif ilaçlarla (m-TOR inhibitörleri) tedavinin devamı denenmelidir.
Diyabet gelişimi:
Yeni başlangıçlı diabetes mellitus sık rastlanan posttransplant karaciğer komplikasyonlarından biridir. Görülme sıklığı değişik serilerde %7- 30 arasında değişmektedir. Bu komplikasyonun etyolojisinde ailede diyabet varlığı, yaşın 45 ten büyük olması, pretransplant glukoz intoleransı olması, santral obezite, metabolik sendrom, uzun süre kortikosteroid kullanımı, takrolimus kullanımı ve hepatit C varlığı sayılabilir. Diyabet gelişimi uzun dönemde kötü graft fonksiyonu dolayısı ile azalmış sağkalımla ilişkilidir. Diyabet gelişimi transplant alıcılarında koroner kalp hastalığı, serebrovasküler hastalık ve periferik oklüziv arter hastalıklarına neden olan önemli bir etkendir. Dolayısı ile önlenmesi ve geliştiğinde de tedavisi önemlidir.
Obezite, Hiperlipidemi ve Metabolik Sendrom:
Obezite karaciğer nakli alıcıları ve donörleri arasında sıklığı gittikçe artmaktadır. Ancak obeziteli hastaların sonuçları şimdilik nonobez olanların sonuçları ile benzerdir. Karaciğer nakli sonrası ilk yıldan sonra mortaliteye neden olan en önemli hastalıklar sırasıyla graft yetmezliği (özellikle HCV nüksü), maligniteler, kardiyovasküler hastalıklar, enfeksiyonlar ve böbrek yetmezliği gelmektedir. Metabolik sendrom posttransplant mortaliteye neden olan bu faktörler için en önemli risk faktörünü oluşturmaktadır. Posttransplant diyabet, posttransplant hipertansiyon ve kriptojenik siroz metabolik sendromla büyük ölçüde ilişkilidir. Bu nedenle karaciğer nakli alıcılarında bu sendrom araştırılmalı ve tedavi edilmelidir.
Primer Hastalık Nüksü:
Primer karaciğer yetmezliğine neden olan etyolojinin nakilden sonra tekrarlaması geç dönem komplikasyonlardan biridir. Viral hepatitlere bağlı etyolojide en fazla nüks HCV de görülmektedir. Çünkü nakilden sonra HCV viremisi saatler içinde başlar ve bu hastaların % 70’inde tekrar kronik hepatit ve karaciğer hasarı oluşabilmektedir. Nakil öncesinde başarılı tedavi ile nakil sonrası HCV nüksü engellenebilmektedir. Günümüzde artık çok başarılı viral tedaviler ile HCV nüksü oldukça düşük seviyelere indirilmiştir. HBV’nün nüks ihtimali de daha az olup bunun nedeni nakil öncesi ve sonrası antiviral tedavi ile nakil sonrası hepatit B immunglobulin (HBIg) tedavisi ile hastalığın tekrarlama ihtimali oldukça azaltılmıştır.
Primer sclerozan kolnajit karaciğer nakillerinin % 5 ini oluşturmasına rağmen nakilden sonra nüks % 10-27 oranında görülebilmektedir. Primer bilier sirozun rekürrens oranı ise daha fazla olup % 50’lere ulaşabilmektedir. Otoimmun hepatitlere yapılan nakil sonrası rekürrens 5 yılda %25, 10 yılda %50 olmakta ancak genellikle hafif seyretmektedir. Bu hasta grubunda akut ve kronik rejeksiyon oranıda daha fazladır. Bu nedenle nakilden sonra immunsupresyon ihtiyacı daha fazladır.
Alkolik sirozlarda yapılan karaciğer nakillerinde posttransplant tekrar alkole başlanma ihtimalini azaltmak için ABD’de çoğu merkezde alkolün en az 6 ay önce bırakma şartı aramaktadır. Nakil sonrası alkole başlama oranları dolayısı ile sirozun nüks etme ihtimali çoğu merkezde farklıdır.
Enfeksiyon:
Enfeksiyon karaciğer nakli hastalarının %60-80’ini etkileyen ve bazen mortaliteye sebep olan ciddi bir komplikasyondur. En sık bakteriyel enfeksiyonlar (gram negatif bakteriler) olmakla birlikte, viral (CMV), fungal (Candida) ve pnöumosystis carini enfeksiyonları görülmektedir. Bakteremia karaciğer nakli hastalarında mortalitenin (%24-36) en önemli sebeplerindendir. Son yıllarda bu oran artmakla birlikte CMV ve fungal enfeksiyon sıklığı azalmaktadır. Karaciğer nakli hastalarındaki bakteriyel enfeksiyonların çoğu nakilden sonraki ilk 1 ay içinde olmakta ve bakteremi insidansı %21-33 arasında değişmektedir. Pek çok merkezde bakretiyel enfeksiyonların % 65’ini intraabdominal veya biliyer kaynaklı gram negatif bakteriler oluşturmaktadır. Risk faktörü olarak diyabet, obezite, akut rejeksiyon, ameliyat süresinin uzunluğu, hipoalbuminemi, pretransplant böbrek yetmezliği, donör özellikleri, hastane florası, yetersiz antibiyotik profilaksisi en önemlileri sayılabilir. Bu tür enfeksiyondan korunmak için rutin ve yeterli posttransplant profilaksi (geniş spektrumlu antibiyotikler ile en az 48 saat olmalı) yapılmalı, yoğunbakımda ve hastanede kalış süresi en aza indirilmeli, kateterler erken çekilmeli ve renal fonksiyonlar düzeltilmelidir (52). Enfeksiyon geliştiğinde de ajana spesifik antibiyoterapi ile tedavi edilmelidir. Posttransplant dönemde enfeksiyonunu önlemek için CMV’de oral valacyclovir veya valgancyclovir, kandidiyazis için nistatin ile, pnöumosystis carini’de ise oral trimethoprim-sulfamethaxasazol ile profilaksi yapılmaktadır. Bu proflaksilerin uygulama süresi merkezler arasında farklılık göstermekle birlikte genellikle 6 ay uygulanmaktadır.
Nörolojik Komplikasyonlar:
Karaciğer naklinin nörolojik komplikasyonları diğer solid organ nakillerinden daha fazla görülmekle birlikte yayınlanan serilerde bu oran %4-70 arasında değişmektedir. Karaciğer nakillerinde fazla olmasının nedeni cerrahi prosedürün komplex olması, nakil bekleyen hastaların genel durum bozukluğu (malnutrisyon, elektrolit bozukluğu, kuagülopati) ve nakil öncesi hepatik ensefalopati varlığı olarak gösterilebilir. Canlı donör karaciğer nakillerinde nörolojik komplikasyonların oranı kadavra vericili nakillerden daha azdır. Bunun nedeni greft kalitesinin iyiliği, kısa soğuk iskemi süresi ve alıcının genel durumunun iyiliği olabilir. Ensefalopati en sık görülen nörolojik komplikasyon olup sebebi; anoksi, primer nonfonksiyon graft, böbrek yetmezliği, rejeksiyon, sepsis, central pontin myelinolysis ve ilaçlardır(kalisinörin inhibitörleri, OKT3 ve steroidler). Epileptik nöbetler ikinci sırada görülmekte olup insidansı % 25-45 arasındadır. Diğer nörolojik komplikasyonlar akut serebrovasküler hastalıklar (%2-6.5) ve intrakraniyal enfeksiyonlardır (%5). Klinikte enfeksiyonlar menenjit, meningo-ensefalit, ensefalit ve beyin abseleri olarak görülmekte olup, mortalitesi oldukça yüksektir.
Graft Versus Host Hastalığı:
Greft Versus Host Hastalığı (GVHD) kemik iliği naklinden sonra sık görülen bir komplikasyon olmakla birlikte karaciğer, böbrek ve ince barsak nakli sonrasında da rapor edilmiştir. Hastalık greft içindeki taşıyıcı lenfositlerin alıcıya taşınması ile oluşmaktadır. Aktarılan bu lenfositler alıcıyı kolonize eder ve alıcı dokularını yabancı antijen olarak tanımaya başlar. Karaciğer nakli hastalarında seyrek (%1’in altında) olarak rastlanmasına rağmen, akut GVHD meydana geldiği zaman genellikle posttransplant periyodun erken döneminde (ilk 5 ay içinde) görülmektedir. Ancak posttransplant geç dönemde (100. günden sonra) bildirilen kronik GVHD vaka sunumları da bulunmaktadır.
Karaciğer nakli hastalarında gelişen GVHD de en sık etkilenen yerler deri ve gastrointestinal sistemdir. Semptomlar olarak desquamatif makulo-papüler döküntü, protein kaybettiren enteropatili kronik diyare ve ateş görülmektedir. Laboratuar çalışmalarında karaciğer fonksiyon testleri normal olup, ciddi lökopeni veya pansitopeni sıklıkla vardır. Tanı için etkilenen bu organlardan alınan doku biyopsileri ve flow sitometri ile dolaşımda verici lenfositlerinin tespiti kullanılmaktadır. Donör ilişkili GVHD da hastalık donör kaynaklı (kendisine yabancı olmadığı için) olduğu için karaciğer etkilenmemektedir. Tedavide agresif immunsupresyon yapılmasına rağmen, GVHD geliştiği zaman genellikle (% 80) ölümcül seyretmektedir ve ölüm genellikle enfeksiyondan olmaktadır.
İnsizyonel Herni:
Ventral insizyonel herniler abdominal cerrahinin en sık komplikasyonlarından biri olup, sıklığı % 4- 20 arasında değişmektedir. İnsizyonel herninin pek çok risk faktörü (hastaya ve cerrahiye ait) tanımlanmış olup bunlar; obezite, ileri yaş, erkek cinsiyet, yara yeri enfeksiyonu, steroid kullanımı, asit varlığı, abdominal distansiyon, sigara içimi, malnutrisyona bağlı kas zayıflığı, diyabet, kollojen doku hastalıkları, periton diyalizi, postoperatif kemoterapi, önceki insizyonların tekrar açılması, trombositopeni veya kuagulopatiye bağlı yara yeri hematomları, acil cerrahi prosedürler, kronik pulmoner hastalıklar, teknik problemler ve yara kapatılması için material kullanımıdır. OLT hastalarında bu risk faktörlerinden çoğu olduğu için insizyonel hernide sık görülebilmekte ve transplant prosedürünü komplike hale getirebilmektedir. Literatürde OLT hastalarında görülme sıklığı % 4.9- 17.2 arasında görüldüğü rapor edilmektedir. Transplant süreci içinde kortikosteroidler hızla azaltılmakta hatta zamanla kesilmekte olmasına rağmen bu komplikasyonun gelişmesini engelleyememektedir. Son zamanlarda immunsupresyon protokollerinde sıkça yer almaya başlayan M-tor inhibitörleri (everolimus ve ya sirolimus) erken postoperatif dönemde kullanıldığında düz kas hücre proliferasyonunu engelleyerek insizyonel herni riskini arttırmaktadır. İnsizyonel herninin tanısı sıklıkla fizik muayene veya gerektiğinde CT kullanımı ile kesinleştirilir.
Günümüzde transplant hastalarının insizyonel hernilerinde laparoskopik mesh herniorafi kullanıldığı rapor edilmesine rağmen genellikle konvansiyonel açık yöntemler kullanılmaktadır. Açık insizyonel herni onarım teknikleri arasında sadece primer sutur veya mesh takviyeli onarımlar yer almaktadır. Mesh yerleştirme teknikleri arasında; primer fascia kapatıldıktan sonra defektin üzerine onlay tekniği, meshin preperitoneal veya prefascial (rektus abdominus kasının arkasında ki retromuskuler alana) tabakaya yerleştirildiği sublay tekniği veya primer fascia kapatmanın mümkün olmadığı defektlerde fascia kenarları arasında bir köprü gibi meshin yerleştirildiği inlay tekniği gösterilmektedir. Mesh kullanılması önerilmektedir. Çünkü mesh, ventral herniorafilerden sonra rekürrensi önlemektedir.
